Лауреатами Нобелевской премии по физиологии и медицине в 2023 году стали Каталин Карико и Дрю Вайсман.
Открытия двух нобелевских лауреатов имели решающее значение для разработки эффективных вакцин мРНК против COVID-19 во время пандемии, которая началась в начале 2020 года. Благодаря своим революционным открытиям, которые фундаментально изменили наше понимание того, как мРНК взаимодействует с нашей иммунной системой, лауреаты внесли свой вклад в беспрецедентным темпам разработки вакцин во время одной из величайших угроз здоровью человека в наше время, говорится в пресс-релизе Нобелевской премии.
Благодаря прогрессу молекулярной биологии в последние десятилетия удалось разработать вакцины на основе отдельных вирусных компонентов, а не целых вирусов. Части вирусного генетического кода, обычно кодирующие белки, находящиеся на поверхности вируса, используются для создания белков, которые стимулируют образование вирусблокирующих антител. Примерами являются вакцины против вируса гепатита В и вируса папилломы человека.
Также части вирусного генетического кода могут быть перенесены в безвредный вирус-носитель, «вектор». Этот метод используется в вакцинах против вируса Эбола. При введении векторных вакцин в наших клетках вырабатывается выбранный вирусный белок, стимулирующий иммунный ответ против целевого вируса.
Биотехнологи: вакцина от рака появится через несколько лет
Производство цельных вирусных, белковых и векторных вакцин требует крупномасштабной культуры клеток. Этот ресурсоемкий процесс ограничивает возможности быстрого производства вакцин в ответ на вспышки и пандемии. Поэтому исследователи уже давно пытались разработать технологии вакцин, независимые от клеточной культуры, но это оказалось сложной задачей.
В наших клетках генетическая информация, закодированная в ДНК, передается на информационную РНК (мРНК), которая используется в качестве матрицы для производства белка. В 1980-е годы были внедрены эффективные методы получения мРНК без культуры клеток, называемые транскрипцией in vitro.
Этот решающий шаг ускорил развитие приложений молекулярной биологии в нескольких областях. Но транскрибируемая in vitro мРНК считалась нестабильной и сложной для доставки, что требовало разработки сложных липидных систем-носителей для инкапсуляции мРНК. Более того, мРНК, полученная in vitro, вызывала воспалительные реакции.
Эти препятствия не обескуражили венгерского биохимика Каталин Карико, которая посвятила себя разработке методов использования мРНК в терапии. В начале 1990-х годов, когда она была доцентом Пенсильванского университета, она оставалась верной своему видению использования мРНК в качестве терапевтического средства, несмотря на трудности с убеждением спонсоров исследований в значимости ее проекта.
Новым коллегой Карико в ее университете стал иммунолог Дрю Вайсман. Его интересовали дендритные клетки, которые выполняют важные функции иммунного надзора и активации иммунных реакций, вызванных вакцинами. Исследователи сосредоточились на изучении того, как различные типы РНК взаимодействуют с иммунной системой.
Карико и Вайсман заметили, что дендритные клетки распознают транскрибируемую мРНК in vitro как чужеродное вещество, что приводит к их активации и высвобождению воспалительных сигнальных молекул. Они задались вопросом, почему транскрибируемая in vitro мРНК была распознана как чужеродная, в то время как мРНК из клеток млекопитающих не вызывала такой же реакции. Карико и Вайсман поняли, что разные типы мРНК должны различаться по некоторым свойствам.
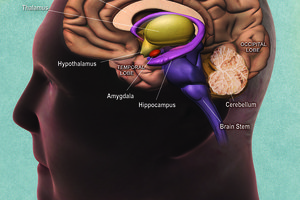
Затяжной COVID-19 и синдром хронической усталости одинаково влияют на мозг: заставляют его стареть
Карико и Вайсман знали, что основания в РНК из клеток млекопитающих часто химически модифицируются, тогда как мРНК, транскрибируемая in vitro, — нет. Они задались вопросом, может ли отсутствие измененных оснований в транскрибируемой in vitro РНК объяснить нежелательную воспалительную реакцию. Чтобы исследовать это, они создали различные варианты мРНК, каждый с уникальными химическими изменениями в основаниях, которые они доставили в дендритные клетки. Результаты были поразительными: воспалительная реакция практически исчезла, когда в мРНК были включены модификации оснований.
Карико и Вайсман сразу поняли, что их открытие имеет огромное значение для использования мРНК в качестве терапии. Эти плодотворные результаты были опубликованы в 2005 году, за пятнадцать лет до пандемии COVID-19.
В дальнейших исследованиях, опубликованных в 2008 и 2010 годах, Карико и Вайсман показали, что доставка мРНК, созданной с модификациями оснований, заметно увеличивает выработку белка по сравнению с немодифицированной мРНК. Эффект был обусловлен снижением активации фермента, регулирующего выработку белка.

На военной базе в Великобритании начали готовиться к пандемии «Болезни Х»
Благодаря открытию того, что базовые модификации одновременно уменьшают воспалительные реакции и увеличивают выработку белка, Карико и Вайсман устранили серьезные препятствия на пути к клиническому применению мРНК.
Интерес к технологии мРНК начал возрастать, и в 2010 году несколько компаний начали разработку этого метода. Продолжалась разработка вакцин против вируса Зика и MERS-CoV, последний из которых тесно связан с с SARS-CoV-2. После вспышки пандемии COVID-19 с рекордной скоростью были разработаны две мРНК-вакцины с модифицированным основанием, кодирующие поверхностный белок SARS-CoV-2. Сообщалось, что защитный эффект составляет около 95%, и обе вакцины были одобрены еще в декабре 2020 года.
Впечатляющая гибкость и скорость, с которой могут быть разработаны мРНК-вакцины, открывают путь к использованию новой платформы для создания вакцин и против других инфекционных заболеваний. В будущем эту технологию также хотят использовать для доставки терапевтических белков и лечения некоторых типов рака.
Читайте также
Нобелевскую премию по медицине присудили за мРНК-вакцины от COVID-19
В США появится первый в мире завод по производству воздушных такси
Бегемоты в пустыне: учёные выяснили, когда и почему Сахара была зелёной
Теперь официально: в Большом адронном коллайдере действительно обнаружили нейтрино
Помощники каждого дня: 7 полезных гаджетов



